Compuṣi Halogenaṭi
2014
Instruire Asistata de Calculator
Prof.Coordonator: Muguras Mocofan
Facultate: Chimie Anul III
Specializarea : CISOPC Grupa: 1B
1.Definitie
Compusii halogenati deriva din hidrocarburi,prin inlocuirea unuia sau mai
multor atomi de hidrogen cu atomi de halogen: fluor,clor,brom,iod.
1.1. Nomenclatura
Denumirea compusilor halogenati se realizeaza astfel:
· Se identifica structura de baza ca fiind cea mai lunga catena alifatica,sau care contine cel mai mare grad de nesaturare;
· Se numeroteaza catena incepand cu substituentii prioritari sau astfel incat suma numerelor de pozitie a substituentilor sa fie cea mai mica;
· Se numesc substituentii in ordine alfabetica,indicand pozitia,numarul si numerele halogenului,inaintea denumirii structurii de baza; numele halogenilor se indica prin prefixele: fluoro-, cloro-, bromo-, iodo- .
2-cloro-3,3-dimetilpentan 1,7-dicloro-4,4-dimetil-6-etil-nonan
Denumiri consacrate de compusi halogenati:
H2C=CH-Cl (C6H5 )3C-Cl H2C=CH-CH2-Cl
Clorura de benzil clorura de vinil clorura de tritil clorura de alil
Clorura de vinil: Policlorura de vinil:
1.2.Metode de obtinere ale compusilor halogenati
Compusii halogenati se obtin prin:
-reactii de substitutie ale atomilor de hidrogen (sau a altor grupe functionale) cu atomi de halogen;
-reactii de aditie ale halogenilor sau hidracizilor la legaturi multiple carbon-carbon (sau la alte legaturi multiple carbon-heteroatom);
-alte reactii (reactii de eliminare,reactii de cloroalchilare).
1.2.1.Obtinerea compusilor halogenati prin reactii de substitutie cu halogeni ale atomilor de hidrogen si ale grupelor functionale 1.2.1.1.Reactii de substitutie cu halogeni ale atomilor de hidrogen
Halogenarea alcanilor
Halogenarea alcanilor se poate realiza cu halogeni in prezenta luminii ultraviolet sau in prezenta peroxizilor, fiind o halogenare homolitica. Etapele reactiei de halogenare (clorurare,in exemplul urmator) sunt:
-etapa de initiere, cand sub actiunea luminii sau a peroxidului, molecula de halogen este scindata in atomi (radicali):
C6H5-CO-O-O-CO-C6H5 → C6H5-COO• → C6H5• + CO2
C6H5• + Cl2 → C6H5Cl + Cl•
-etapa de propagare, in care radicalul (atomul de halogen) reactineaza cu catena alifatica, formand un alt radical si o molecula de hidracid; radicalul format scindeaza o alta mlecula de halogen formand compusul halogenat si un alt atom de halogen. Reactia de propagare continua pana la consumarea materiilor prime sau pana la inhibarea reactiei.
CH4 + Cl• → CH3• + HCl CH3• + Cl2 → CH3Cl + Cl•
Clorura de metil
CH3Cl + Cl• → CH2Cl• + HCl CH2Cl• + Cl2 → CH2Cl2 + Cl•
Clorura de metilen
CH2Cl2 + Cl• → CHCl2• + HCl CHCl2• + Cl2 → CHCl3 + Cl•
Triclorometan(cloroform)
CHCl3 + Cl• → CCl3• + HCl CCl3• + Cl2 → CCl4 + Cl•
Tetraclorura de carbon
-etapa de blocare consta in reactia dintre doi radicali identici sau diferiti.
Cl• + Cl• → Cl2 CH3• + CH3• →CH3-CH3 CH3• + Cl• → CH3Cl
Reactivitatea halogenilor in reactiile homolitice scade de la fluor la iod, in timp ce selectivitatea creste de la fluor la iod:
 Reactivitate
Reactivitate
F2 Cl2 Br2 I2
 Selectivitate
Selectivitate
Reactivitatea atomilor de hydrogen din catenele alifatice depinde de natura atomului de carbon de care este legat, ordinea reactivitatii fiind:
H-C tertiar > H-C secundar > H-C primar > CH4
Ca agenti de halogenare mai pot fi folositi: clorura de sulfuril (SO2Cl2), fosgenul (COCl2), pentaclorura de fosfor (PCl5), N-bromosuccinimida, clorura de oxalil (ClOC-COCl), t-butil-hipocloritul sau hipobromitul (t-BuOCl, t-BuOBr).
In reactiile de clorurare homolitica ale alcanilor se formeaza, in general, amestecuri de produsi monohalogenati izomeri si compusi polihalogenati, selectivitatea reactiei fiind redusa. Astfel la monoclorurarea 2-metilbutanului (izobutanului) la 300°C se formeaza urmatorul amestec de compusi monoclorurati:
CH3-CH2-CH-CH3 →Cl-CH2-CH2-CH-CH3 +CH3-CH-CH-CH3 +
CH3 16,5% CH3 28% CH3
4-cloro-2-metilbutan 3-cloro-2-metilbutan
Cl
+ CH3-CH2-C-CH3 + CH3-CH2-CH-CH2-Cl
22% CH3 33% CH3
2-cloro-2-metilbutan 1-cloro-2-metilbutan
Bromul fiind mai putin reactiv decat clorul, selectivitatea reactiilor de bromurare este mai mare. Astfel la bromurarea propanului cu brom la 127 °C in prezenta luminii se formeaza majoritar 2-bromopropanul, in timp ce la bromurarea izobutanului se formeaza, practic cantitativ, 2-bromo-2-metilbutanul.
Halogenarea in pozitia alilica
Halogenarea in pozitia alilica se poate realize cu clor sau cu brom la temperaturi ridicate (400-600°C). Astfel, propena tratata cu clor sau cu brom la 300-400°C formeaza clorura, respectiv bromura de alil.
H2C=CH-CH3 → X2 H2C=CH-CH2-X + HX X=Cl, Br

Pozitia alilica
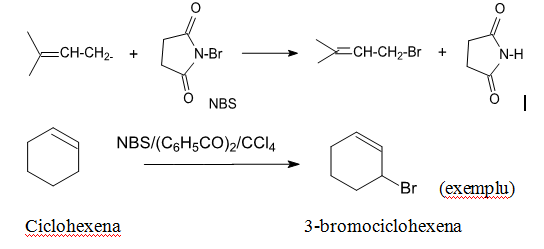
Bromurarea in pozitia alilica ae poate realize la incalzire cu bromosuccinimida (NBS), in prezenta luminii sau a generatorilor de radicali [(C6H5CO)2O2 peroxid de benzoil, (H3C)2C(CN)-N=N-C(CN)C(CH3)2 azoizobutironitril], folosind ca mediu de reactive CCl4, in care doar succinimida formata este insolubila. N-Bromosuccinimida prezinta avantajul ca in reactie nu se formeaza acid bromhidric si astfel nu se vor forma produsi de aditie la dubla legatura.
Halogenarea in pozitia benzilica
La tratarea toluenului cu clor ( sau brom), la temperatura de reflux, in prezenta luminii solare sau a luminii ultraviolet, dar in absenta catalizatorilor, are loc halogenarea in catena lateral, cu formarea clorurii de benzil. Folosind exces de clor se formeaza clorura de benziliden si fenil-triclorometan.
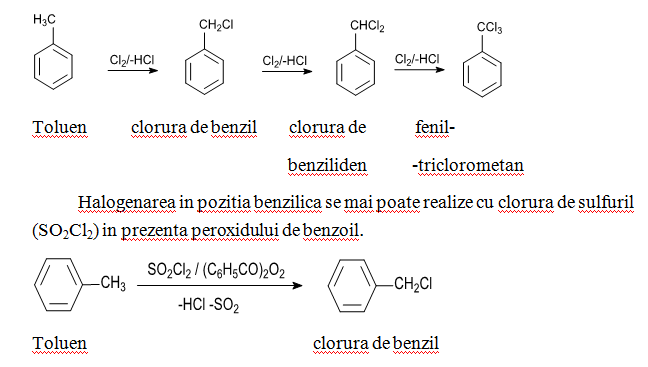
Clorura de benzil:
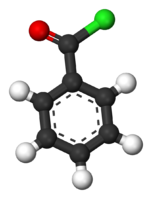
Bromurarea in pozitia benzilica se mai poate realize cu ajutorul NBS in prezenta peroxidului de benzoil, de obicei in tetraclorura de carbon; se pot bromura in catena lateral, toluenii substituiti, metilnaftalenul, alchil-benzenii, etc.
Halogenarea hidrocarburilor aromatice si a compusilor aromatici
Halogenarea hidrocarburilor aromatice si a compusilor aromatici la nucleu se realizeaza in absenta sau in prezenta catalizatorilor (FeCl3, Fe, AlCl3, AlBr3, I2), fiind o reactie de substitutie electrofila. Mecanismul reactiei presupune formarea, in prima etapa, a unui complex cu transfer de sarcina (complex π), care trece in complexul de tip σ (cation de benzenoniu),din care prin eliminarea unui proton se reface starea aromatic.
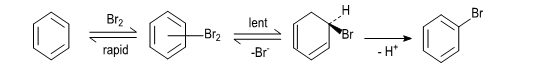
Complex π complex σ
Vitezareactiilor este marita prin utilizarea catalizatorilor, mai ales in cazul compusilor aromatici cu reactivitate redusa. Catalizatorii folositi (catalizatori de tip Lewis) polarizeaza sau chiar scindeaza molecula halogenilor; cationii de halogen formati fiind agenti electrofili mai energici decat halogenul in absenta catalizatorului.
Cl - Cl + FeCl3 ↔ Clδ+ - - Clδ- - - FeCl3 ↔ Cl+ [FeCl4]-
Benzenul nu reactioneaza cu clorul sau bromul la rece, dar in prezenta catalizatorilor (clorura de aluminiu, fier, piridina) reactia are loc cu usurinta, cu formarea, mai ales, a compusului monohalogenat.
Compusii aromatici reactivi (care poseda substituenti cu effect respingator sau donor de electroni +I, +M; exemplu: -R, -OH, OR, -NH2, -NHR), nu necesita catalizatori in reactiile de halogenare,datorita cresterii densitatii de electroni in pozitiile orto si para. Astfel anilina si fenolul se pot triclorura (tribromura) chiar in solutie apoasa.
Alte caracteristici ale reactiei de halogenare ale hidrocarburilor aromatice
Rolul catalizatorului in reactiile de halogenare ale hidrocarburilor aromatice este de a creste electrofilicitatea halogenilor. Astfel benzenul se bromureaza cu brom, in prezenta piridinei, in conditii blande:
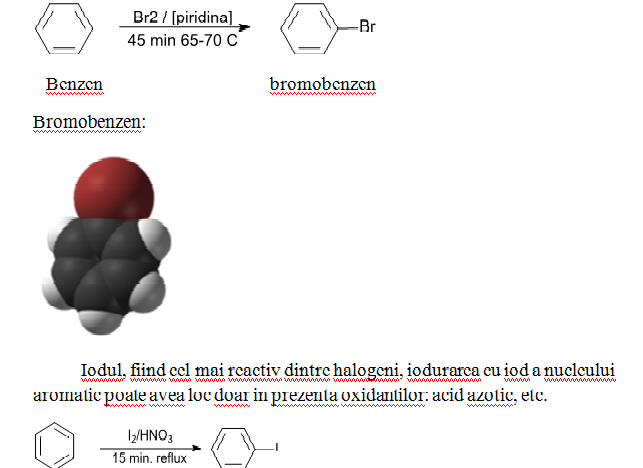
benzen iodobenzen
Halogenarea fenolilor
Datorita efectului activant al grupei hidroxi fenolice, la tratarea cu brom a unei solutii apoase de fenol, precipita imediat 2,4-tribromofenolul; similar, la tratarea unei solutii fenolice cu clor, la cald, se formeaza 2,4,6-triclorofenolul.
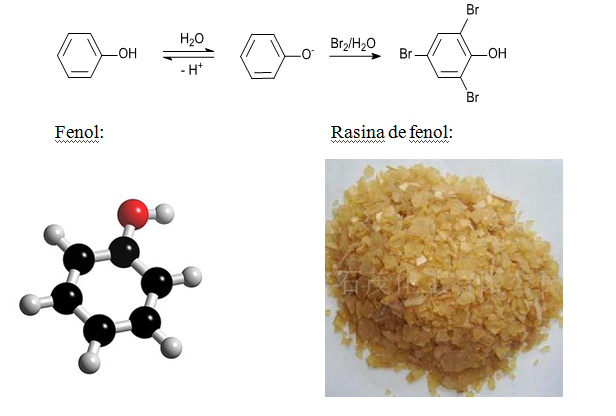
Pentru a obtine monobromofenolul, bromurarea fenolului se efectueaza la 0-5°C in solvent aprotici, cum ar fi sulfura de carbon sau tetraclorura de carbon (care nu permit formarea ionului fenolat; deci activarea nucleului benzenic va fi mai redusa ca in solutie apoasa); in aceste conditii se formeaza majoritar p-bromofenolul.
Halogenarea anilinelor
Datorita efectului activant al grupei amino, la tratarea anilinei cu brom sau clor in solutie apoasa se produce tribromurarea, respectiv triclorurarea.
Pentru a obtine aniline monohalogenate se utilizeaza agenti de halogenare mai blanzi (N-clorosuccinimida) sau efectrofili mai blanzi: iod (in prezenta bazelor, pentru fixarea HI format).
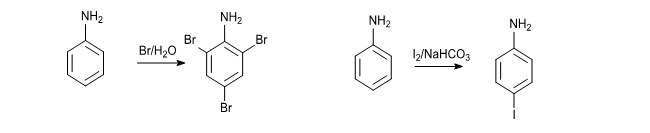
Halogenarea compusilor aromatic cu substituenti diferiti
In cazul prezentei pe nucleul aromatic a substituentilor cu efecte electronice diferite (-I, +I, -M, +M), orientarea halogenarii va fi determinate de substituentul cu efect donor (sau respingator) de electroni, insa reactivitatea compusului va fi mai scazuta. Astfel clorurarea 4-nitro- si 3-nitrotoluenului necesita temperatura mai mare decat clorurarea toluenului. In primul caz se formeaza un singur produs:
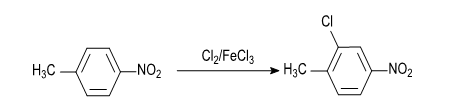
4-nitrotoluen 2-cloro-4-nitrotoluen
in timp ce in al doilea caz un amestec de izomeri monoclorurati:
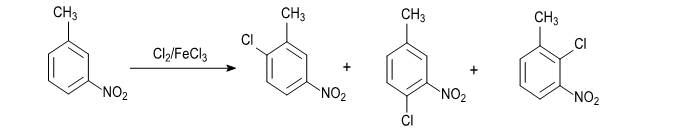
3-nitrotoluen 6-cloro- 4-cloro-3- 2-cloro-3-
-3-nitrotoluen -nitrotoluen -nitrotoluen
3-nitrotoluen:
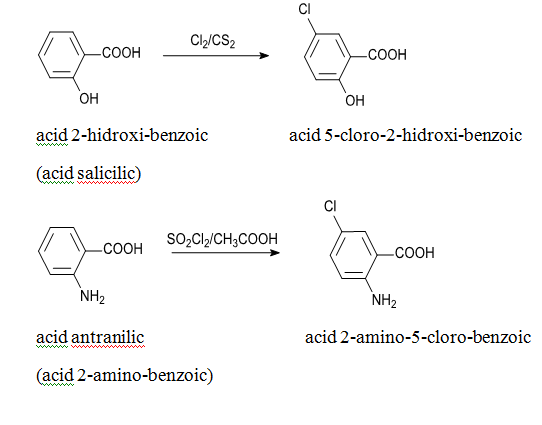
Acidul salicilic se monoclorureaza la 10-15°C in CS2 , cu formarea acidului 5-clorosalicilic; acidul antranilic se monoclorureaza cu clorura de sulfuril in prezenta acetatului de sodium, la 25°C, sau se diclorureaza cu clor in acid acetic la 25°C.
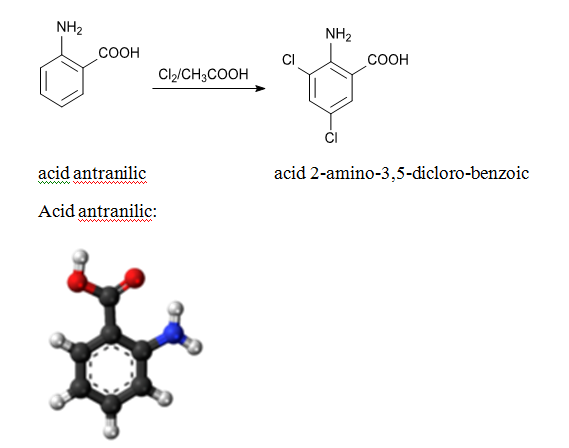
Halogenarea compusilor cu hidrogen active (halogenarea compusilor carbonilici, acizilor carboxilici, sulfonelor si sulfoxizilor, cetoximelor si a aldoximelor, nitroderivatilor alifatici)
Halogenarea compusilor cu hidrogen activ se realizeaza in conditii si cu catalizatori specifici pentru: compusii carbonilici (aldehide si cetone), acizi carboxilici, sulfone si sulfoxizi, aldoxime si cetoxime,nitro derivati alifatici.
Halogenarea compusilor carbonilici
Halogenarea compusilor carbonilici se realizeaza cu clorura de sulfuril (SO2Cl2), clorura cuprica (CuCl2), bromura cuprica (CuBr2), N-bromosuccinimida
(NBS), halogeni in solvent organic sau, in cazul cetonelor alifatice, cu clor, in mediu apos, in prezenta carbonatului de calciu.
Prin actiunea bromului asupra acetone, in functie de conditiile de reactive, se poate obtine 1-bromoacetona, 1,3-dibromoacetona sau 1,1,3-tribromoacetona.
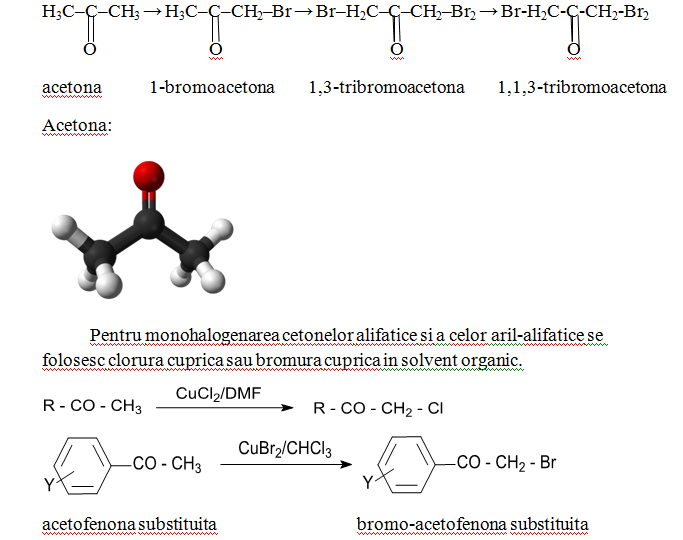
Halogenarea cetoximelor si a aldoximelor
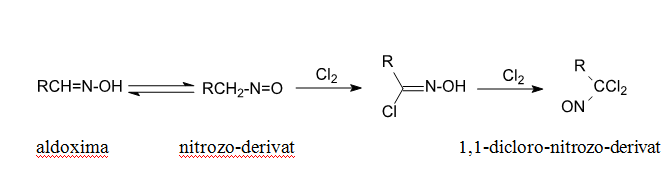
Halogenarea cetoximelor si a aldoximelor are loc la atomul de carbon la care este legata grupa oximica si conduce la halogeno-nitrozo derivati geminali.
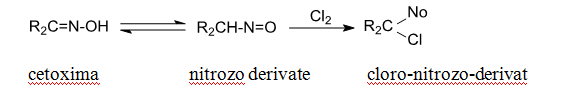
6.2.1.2.Reactii de substitutie a atomilor de halogen cu halogeni
Reactia de interschimb a halogenilor (metoda Finkelstein) este o reactie reversibila de substitutie nucleofila, bazata pe diferenta de nucleofilicitate a anionilor de halogenura. Nucleofilicitatea anionilor de halogenura creste odata cu scaderea electronegativitatii halogenilor: F < Cl < Br < I.
RX + X'- ↔ RX' + X-
Deplasarea echilibrului in sensul formarii iodurilor de alchil se bazeaza pe solubilitatea NaI in acetona si insolubilitatea NaCl sau NaBr in acetona.
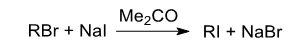
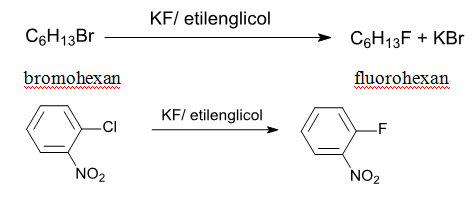
Compusii florurati se pot obtine prin tratarea compusilor clorurati, bromurati sau iodurati cu fluoruri anorganice (AgF, KF, HgF2) in etilenglicol la 160°C. Deplasarea echilibrului in sensul formarii compusului fluorurat se bazeaza pet aria legaturii C-F, care odata formata nu mai poate fi scindata usor.
6.2.1.3.Reactii de substitutie cu halogeni ale grupelor functionale cu continut de oxygen
Obtinerea compusilor halogenati din alcooli
R - OH → R - X
Reactia de substitutie a grupei -OH din alcooli este o reactie de substitutie nucleofila, care poate avea loc prin mecanism monomolecular (SN1) sau bimolecular (SN2). Reactivitatea alcoolilor in reactia de inlocuire a grupei hidroxi cu halogen, descreste in ordinea:
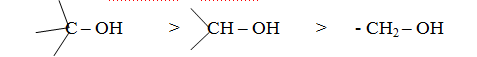
alcool tertiar alcool secundar alcool primar
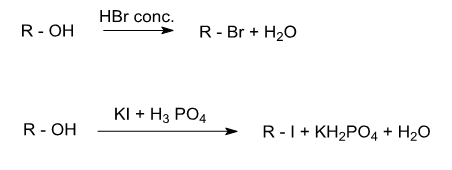
Practic, transformarea alcoolilor in compusi halogenati se poate realize cu :
a) solutii apoase de hidracizi concentrate (HBr sau HCl in prezenta ZnCl2), hidracizi in stare gazoasa (HCl, HBr). Pentru obtinerea iodurilor se foloseste KI si acid fosforic.
b) halogenuri alcaline (NaBr, NaCl, KBr, KCl) in prezenta H2SO4 conc. in exces
NaBr:

c) halogenuri si oxihalogenuri ale fosforului [tribromura sau pentabromura de fosfor (PBr3, PBr5 ), triclorura de fosfor (PCl3), oxitriclorura de fosfor (POCl3)]
![]()
d) oxihalogenuri ale sulfului [clorura sau bromura de tionil (SOCl2, SOBr2)] in prezenta piridinei
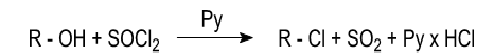
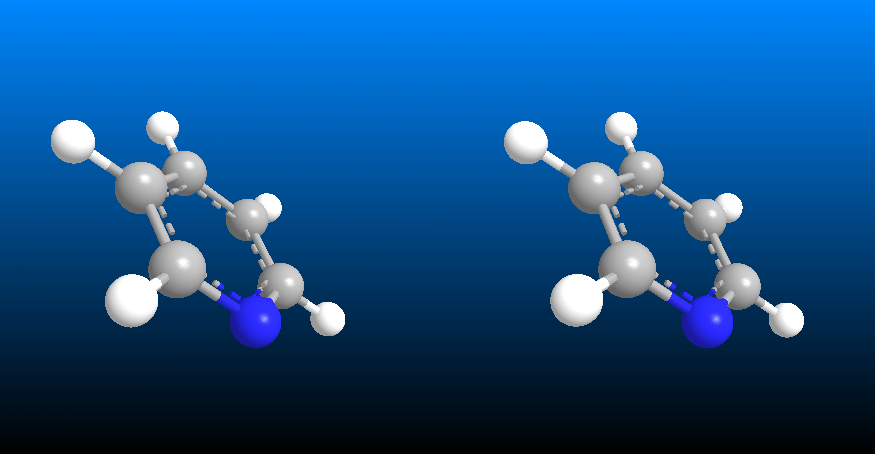
Piridina:
e) trifenilfosfin-diclorura sau dibromura {[P(C6H5)3]Cl2 sau [P(C6H5)3]Br2} sau trifenilfosfina [P(C6H5)3] in CCl4, CBr4.
R - OH + (C6H5)3PBr2 → R - Br + (C6H5)3PO + HBr
trifenilfosfin bromura trifenilfosfinoxid
R - OH + (C6H5)3P + CBr4 → DMF R - Br + (C6H5)3PO + CHBr3
trifenilfosfina trifenilfosfinoxid
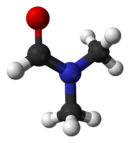
Dimetilformamida:
f) iod si fosfor rosu sau brom si fosfor rosu
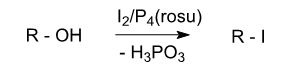
Fosfor rosu:

g) tetrafluorura de sulf (SF4)
Exemple:
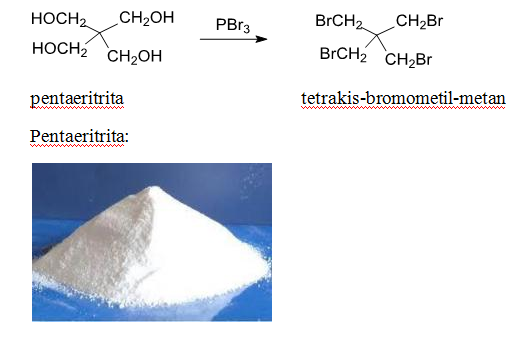
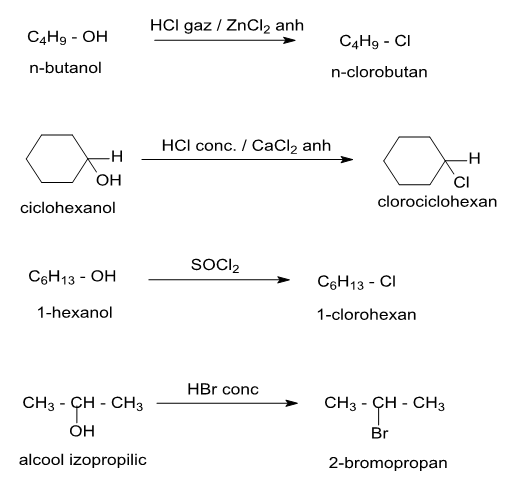
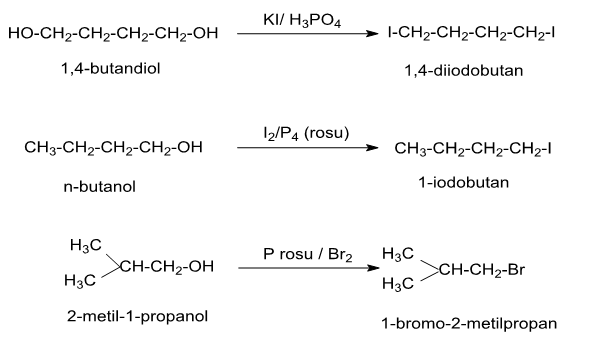
- Teacher: Muguras Mocofan
- Teacher: Ileana Rosca